Атомы элементов, имеющие на внешнем уровне шесть, семь
электронов, легко принимают недостающие до восьми электроны, проявляя
свойства окислителей. Особенно сильными окислительными свойствами обладают
галогены F2,
Сl12
Вг2,
J2
и кислород О2.
Элементы в высшей степени окисления, равной номеру группы, могут быть
только окислителями, могут только принимать электроны, восстанавливаясь
при этом. Например, сера (элемент VI группы) в соединении H2SO4
находится в высшей степени окисления, равной +6. На внешнем уровне S-6
нет электронов: S-6
Is22s22p63s03p0,
пoэтому S+6
может только принимать электроны, выполняя роль окислителя в окислительно-восстановительных
реакциях.
К важнейшим окислителям относятся:
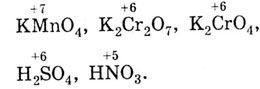
Степень окисления центрального атома в этих соединениях соответствует
номеру группы.
|