Степень окисления - это условный
заряд атома в молекуле, если считать, что все молекулы состоят из ионов.
Степень окисления рассчитывается алгебраически, учитывая, что сумма положительных
и отрицательных зарядов в молекуле равна нулю.
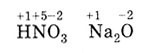
Задача. Напишите электронную конфигурацию
иона Со+2
и иона Co+3.
Ответ. Кобальт (элемент с атомным номером
27) имеет электронную конфигурацию [Ar] 4s23d7.
Для образования иона с зарядом +2 атом кобальта должен отдать два электрона.
Сначала происходит потеря 4s-электронов, а затем 3d-электронов. Следовательно,
ион Со+2
должен иметь электронную конфигурацию [Аr] 3d7.
Для образования иона Со+3требуется
отнять еще один электрон. Поэтому кобальт-ион Со+3
должен иметь электронную конфигурацию [Аr] 3d6.
Задача. Укажите тип химической связи и объясните
формулы следующих водородных соединений: NaH, MgH2,
АlН3,
SiH4,
PH3, H2S,
HCl.
Ответ. Гидриды металлов представляют собой ионные соединения, состоящие
из катионов металлов и гидрид-ионов Н-.
Стремясь приобрести электронную конфигурацию благородного газа, атом натрия
отдает один электрон (Na0
——> Na+
+ 1е-),
магний отдает два электрона (Mg0
—-> Mg+2
+ 2e-
), алюминий отдает три электрона (Аl0
—-> Аl+3
+ Зе-).
На каждый отданный электрон приходится один гидрид-ион (Н0
+ 1е-
—-> Н-).
Следовательно, три первых соединения отвечают составу Na+H-,
Mg+22H-,
Al+33H-.
Остальные соединения лучше рассматривать как ковалентные полярные, в которых
происходит обобществление электронной пары между центральным атомом и
каждым атомом водорода. Атому кремния, элементу группы 4А, требуется 4
электрона, чтобы приобрести конфигурацию благородного газа из восьми валентных
электронов. Атому фосфора необходимо три электрона, сере - два, а хлору
— один электрон. Формулы водородных соединений находятся в соответствии
с числом электронов, необходимых для завершения октета.
|