 |
| Общая химия. |
| Строение атома. Химическая связь. |
| Характеристика 4 квантовых чисел. |
| |
| |
- Главное квантовое число (n) — характеризует энергию и размер орбитали.
Оно принимает значения от 1 до
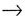 :
n = 1, 2, 3, 4, 5, 6, 7. :
n = 1, 2, 3, 4, 5, 6, 7.
- Побочное (орбитальное) квантовое число (1) - характеризует форму
орбиталей и принимает значения от 0 до (n - 1): 1 = О, 1, 2, 3, 4. Например,
если n = 2, то 1 имеет 2 значения: О, 1. Значит, на 2 энергетическом
уровне есть сферическая орбиталь (1 = 0) и в виде объемной восьмерки
(гантелеобразная) (1 = 1).
- Магнитное квантовое число (m) - характеризует количество орбиталей
одинаковой формы и ориентацию их в электромагнитном поле ядра атома.
Оно принимает значения в интервале от —1 до +1. Для каждого значения
разрешено (21 + 1) значений числа m. Например, если 1 = 1, то m имеет
(2 x 1 + 1) 3 значения: — 1,0, +1.
- Спиновое квантовое число (s) - характеризует вращение электрона вокруг
своей оси и принимает только 2 значения: +1/2 (
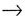 )
и -1/2 ( )
и -1/2 (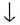 ). (Спин электрона
— свойство электрона вести себя как крошечный магнит). ). (Спин электрона
— свойство электрона вести себя как крошечный магнит).
|
| |
 |
|